1. 서 론
2. 주석 페로브스카이트에 대한 기초적 지식
2.1 주석 원자의 기본적인 성질
2.2 주석 페로브스카이트의 기본적인 성질
3. 주석 페로브스카이트 태양전지
3.1 주석 페로브스카이트 태양전지의 활용방안과 문제점
3.2 주석 페로브스카이트 태양전지의 문제 해결 전략
4. 결 론
1. 서 론
할라이드 페로브스카이트는 ABX3 결정 구조를 가진 물질을 일컫는 말로, Fig. 1a에서 볼 수 있듯이 A는 포름-아미디늄 (FA+), 메틸-암모늄(MA+)과 같은 1가 양이온, B는 Ge2+, Pb2+, Sn2+와 같은 2가 양이온, X는 Cl-, Br-, I-와 같은 1가 할라이드 음이온으로 구성되어 있다. 할라이드 페로브스카이트는 낮은 엑시톤 속박 에너지와 높은 흡광 계수, 높은 캐리어 이동도, 밴드갭이 조절 가능하다는 점 등 다양한 장점으로 인해 태양전지와 발광 다이오드, 레이저를 포함한 다양한 소자에서 많은 관심을 받고 있다1-7). 특히 Miyasaka 그룹이 할라이드 페로브스카이트를 태양전지의 광활성층으로 사용할 수 있다는 가능성을 보고한 이후, 할라이드 페로브스카이트를 태양전지로 활용하는 연구가 기대를 받고 많은 발전을 이뤘으며 현재 25%가 넘는 전력 변환 효율을 가지는 페로브스카이트 태양전지가 보고되고 있다5,8). 높은 전력 변환 효율을 가지고 있으며 저비용 공정이라는 장점에도 불구하고, 페로브스카이트 태양전지는 아직 상용화가 불가능한데 이는 실리콘 태양전지에 비해 낮은 안정성, 대면적화, 납의 독성과 같이 아직 해결해야 할 요소들이 많이 존재하기 때문이다9-11). 특히 납의 독성은 페로브스카이트 태양전지가 상용화되기 위해 필수적으로 해결해야 하는 요소인데, 현재 보고되고 있는 대부분의 고효율 및 고안정성 페로브스카이트 태양전지는 납 페로브스카이트 태양전지이므로 납을 독성이 덜한 다른 물질로 대체하는 것이 필요하다.
많은 연구진들은 납을 대체하기 위해 같은 14족에 위치하는 저마늄과 주석을 통해 그리고 15족에 위치하는 비스무스와 안티모니를 통해 페로브스카이트 태양전지를 개발하는 연구를 진행하였다(Fig. 1b)12,13). 그 이외에도 두 개 이상의 금속 양이온이 페로브스카이트의 B 위치에 존재하는 더블-페로브스카이트나 란타나이드, 알칼리 토금속으로 페로브스카이트를 만들고 이를 통해 납이 없는 페로브스카이트 태양전지를 제작하려는 연구 또한 진행되었다(Fig. 1c)13-16). 이러한 노력에도 불구하고, 위에서 언급한 물질 대부분은 납이 없는 페로브스카이트 태양전지를 만들기에 적합하지 않으며 그 이유는 다음과 같다. 먼저 광활성상을 가지는 결정 구조가 특정되어 있다는 것이다. 원자의 크기와 산화 상태에 따라 결정 구조를 알 수 있는 골드슈미트 공차 계수에 의하면, 광활성상이면서 안정적인 구조를 가지기 위해서는 골드슈미트 공차 계수가 0.8과 1.0 사이여야 하고 이로 인해 페로브스카이트 태양전지로 적절한 원자 종류에 한계가 존재한다17). 페로브스카이트 태양전지로 활용할 수 있는 물질에 제약이 있는 또 다른 이유로는 물질의 안정성과 적절한 광학적 특성을 동시에 가지는 페로브스카이트를 찾기 어렵다는 점이다. 15족에 위치하는 비스무스와 안티모니는 3가 양이온이기 때문에 단독으로 사용할 경우 2가 양이온인 납과 달리 구조에 결함을 필수적으로 가져온다는 점, 더블 페로브스카이트를 사용할 경우 결함이 없고 물질의 안정성은 뛰어나지만 간접 밴드갭을 형성한다는 점, 저마늄을 이용할 경우 직접 밴드갭을 갖지만 4s 오비탈의 전자배치를 가져 전자들을 쉽게 잃을 수 있어 화학적 안정성이 나쁘다는 점을 그 예로 들 수 있다(Fig. 1d)18-20).
따라서 납이 없는 페로브스카이트에 대한 많은 연구가 진행되었지만, 직접 밴드갭 구조와 동시에 뛰어난 전자적 특성 및 광학적 특성을 가지는 주석이 태양전지 분야에서 납을 대체할 가능성이 가장 높은 물질로 여겨지고 있다. 실제로 2014년 Hao와 공동 연구자들이 5.73%의 효율을 가지는 주석 페로브스카이트 태양전지를 처음 보고한 이후, 많은 발전을 이뤄 Zhubing과 Jiang이 각각 14.81% (인증 효율 14.03%)와 인증 효율 14.6%에 해당하는 효율을 달성하였다(Fig. 1e)21-23). 해당 효율은 납이 없는 페로브스카이트 태양전지 중 가장 높은 효율이며 이는 주석 페로브스카이트 태양전지의 가능성을 뒷받침한다. 주석 페로브스카이트 태양전지가 납이 없는 다른 종류의 페로브스카이트 기반의 태양전지에 비해 높은 효율을 보이는 이유는 납 페로브스카이트 태양전지와의 유사성에서 찾을 수 있다. 주석은 납과 유사한 ns2 전자배치를 가지며 같은 2가 양이온을 형성하는 원자이며, 차이가 크지 않은 원자 크기를 가지고 있어 골드슈미트 공차 계수를 쉽게 맞출 수 있다24). 그 이외에도 다른 종류의 납이 없는 페로브스카이트와 달리 적절한 직접 밴드갭을 가지고 있고 높은 캐리어 이동도와 좋은 광학적 특성을 가지는 것 또한 페로브스카이트 태양전지로 사용하는데 긍정적인 요소이다25,26).
그러나 15%에 이르는 주석 페로브스카이트 태양전지의 효율은 기존의 납 페로브스카이트 태양전지에 비하면 여전히 낮은 효율이며, 따라서 Fig. 1f에서 볼 수 있듯이 주석의 불안정성 및 부적절한 에너지 준위를 가진 전하 수송층을 개선하는 전략들이 제안되었다27). 주석은 Sn2+가 Sn4+로 산화되는 현상이 납보다 쉽게 일어날 수 있고, Sn4+이 만들어질수록 결함이 더 많아지므로 더 낮은 성능을 보인다28). 현재 주석 페로브스카이트 태양전지에서는 납 페로브스카이트 태양전지에 사용되었던 수송층 중 주석 페로브스카이트와 에너지 준위가 그나마 일치하는 것으로 사용하고 있다22,23). 하지만 이는 적절한 에너지 준위를 가진 수송층을 사용하는 것이 아니므로 재결합이 발생하는 요소로 작용한다.
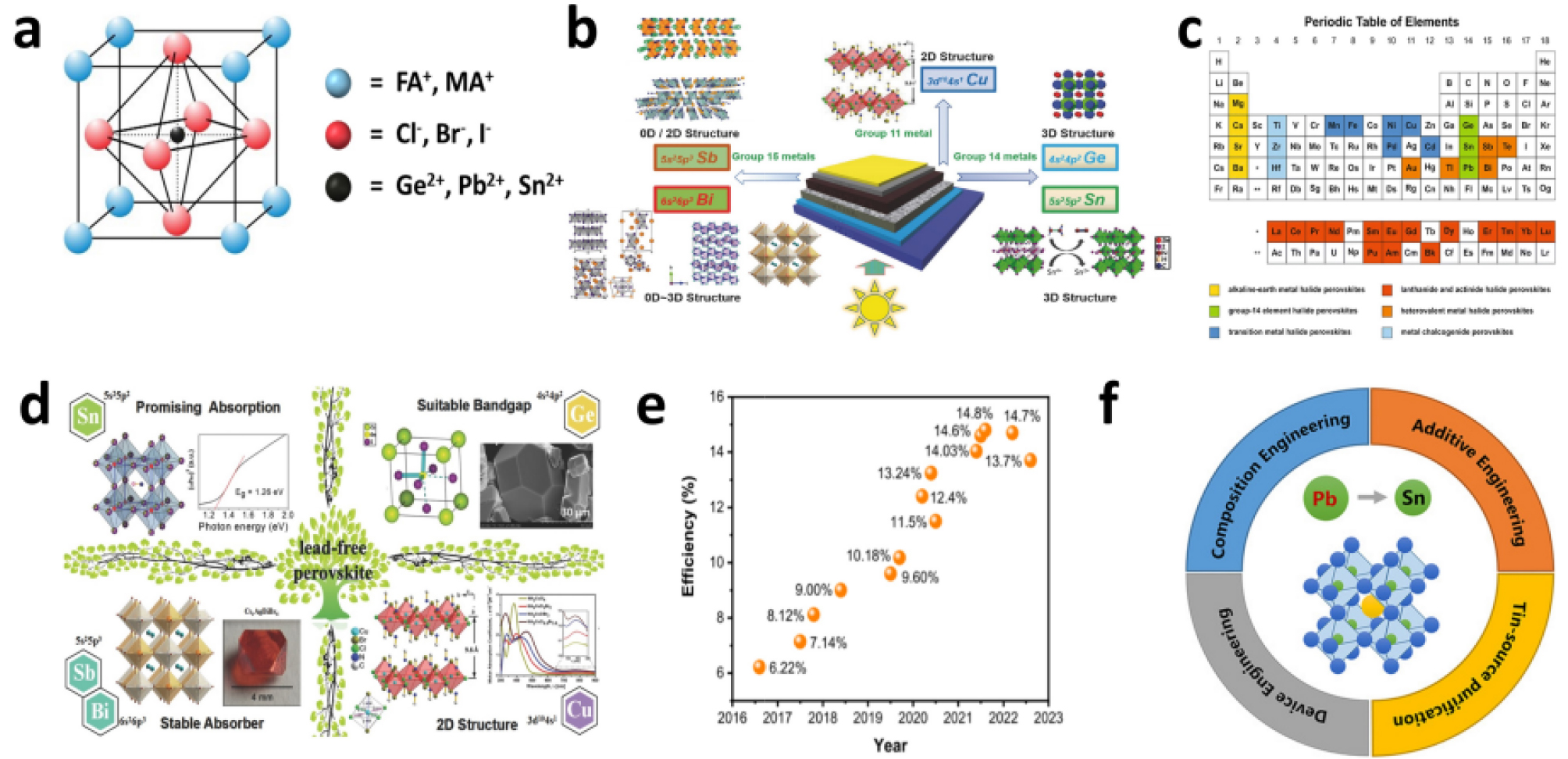
Fig. 1
(a) Structure of halide based perovskite. (b) Elements applicable to the perovskite structure12). (c) Element candidates that can be used as lead-free perovskites14). (d) Characteristics of lead-free perovskites19). (e) Highest efficiency of tin perovskite solar cells by year21). (f) Main strategies for stable tin perovskite solar cells27).
이 글에서는, 주석 페로브스카이트와 주석 페로브스카이트 태양전지에 대한 전반적인 개요를 보여주고자 한다. 먼저 주석 페로브스카이트의 종류 및 구조와 전자적 특성, 광학적 특성 등 태양전지와 관련된 기본적인 특성을 납과 비교해 알아본다. 납과의 비교 및 분석을 하는 이유는 납 페로브스카이트 태양전지가 현재 가장 좋은 성능을 보이기 때문에 주석의 장점과 단점을 명확히 확인할 수 있기 때문이다. 그 후 주석 페로브스카이트 태양전지의 현재 문제점에 대해 살펴보고 이를 해결하기 위한 노력에 대해 살펴본다. 마지막으로는 여전히 남아있는 문제점 그리고 주석 페로브스카이트 태양전지에 전망에 대해 논의할 것이다.
2. 주석 페로브스카이트에 대한 기초적 지식
주석은 납과 같은 14족에 위치하기 때문에 다른 종류의 페로브스카이트과 달리 납 페로브스카이트와 비슷한 물리적 성질과 화학적 성질을 가지고 있다. 그럼에도 불구하고, 원자 크기의 차이로 인해 납 페로브스카이트와는 또다른 특성을 보인다. 따라서 주석 페로브스카이트 태양전지에 대해 이해하기 위해서는 원자 단위부터 페로브스카이트 결정 단위까지 어떤 공통점 및 차이점이 있는지 그리고 주석으로 인한 고유의 특징으로는 무엇이 있는지를 아는 것이 중요하다. 따라서 이번 장에서는 납과의 비교분석을 통해 주석 원자의 기본적인 특징과 주석 페로브스카이트의 기본적인 특성 등에 대해 알아보고자 한다.
2.1 주석 원자의 기본적인 성질
주석은 원자번호 50번에 해당하는 전이금속으로, 납과 같이 14족에 위치해 있다. 납의 원자번호가 더 크기 때문에 주석의 전자배치에서 볼 수 없는 f 오비탈이 납의 전자배치에서 존재하지만, 주석과 납 모두 원자가전자가 ns2np2로 같다는 것이 특징이다(Table 1). 이로 인해 가능한 산화 상태로는 np2 오비탈의 전자를 잃는 +2와 ns2np2 오비탈의 전자를 모두 잃는 +4가 있다. 특이한 점은 주석과 납의 가장 안정한 산화 상태가 다르다는 것인데, 주석은 +4 산화 상태를 가질 때 더 안정한 상태를 가지는 반면 납은 +2의 산화 상태를 가질 때 더 안정한 상태를 가지게 된다27). 이는 란타나이트 축소에 따른 비활성 전자쌍 효과로 설명 가능하다. 란타나이트 축소는 4f 오비탈의 핵전하 가리움 효과가 좋지 않아 최외각에 존재하는 전자가 더 큰 유효 핵전하를 느끼는 것을 말하고 비활성 전자쌍 효과는 최외각에 존재하는 s 오비탈의 전자 두 개가 공유되거나 이온화되지 않고 그대로 안정화되는 현상을 말한다29-31). Table 1에서 확인할 수 있듯이, 주석과 달리 납은 4f 오비탈이 존재하기 때문에 최외각 전자에 대한 가리움 효과가 적고 유효핵전하가 커서 최외각에 존재하는 s 오비탈이 비교적 안정화되는 것이다. 그 결과 납은 주석과 달리 +2 산화 상태에서 더 안정적인 구조를 이루게 된다. 실제로 비활성 전자쌍 효과의 정도를 정량화할 수 있는 4번째 전자가 이온화되는 데까지 필요한 이온화에너지를 계산해보면 주석은 8,991.3 kJ/mol, 납은 9,328.4 kJ/mol로 주석이 +4 산화 상태가 되는 것이 더 쉬운 것을 확인할 수 있다.
주목해야 할 두 번째 요소는 이온 반지름이다. 원자 번호와 전자 배치를 보면 주석이 납보다 더 작은 크기를 가질 것이라 예상할 수 있다. 실제로 주석은 +2 산화 상태에서 1.12Å, +4에서 0.70 Å의 원자 크기를 가지고 납은 +2 산화 상태에서 1.32Å, +4에서는 0.84Å의 원자 크기로 주석이 산화 상태와 관계없이 더 작은 이온 반지름을 가지는 것을 확인할 수 있다(Table 1). 비록 원자 단위에서는 주석의 작은 크기가 큰 영향이 없지만, 페로브스카이트 단위에서 주석의 작은 크기는 주석 페로브스카이트를 이룰 수 있는 물질의 종류가 납 페로브스카이트와 달라지는 원인이 된다. 그 이외에도 골드슈미트 공차 계수와 정팔면체 계수에 영향을 미쳐 광활성 구조를 이루는 데에도 영향을 미친다. 이에 대한 자세한 내용은 주석 페로브스카이트 부분에서 다룰 것이다.
Table 1.
Comparison of basic information of tin and lead atoms
2.2 주석 페로브스카이트의 기본적인 성질
2.2.1 페로브스카이트의 결정 구조
페로브스카이트의 ABX3 구조는 일반적으로 [BX6]4- 정팔면체가 모서리 공유를 하고 A 양이온이 [BX6]4- 사이 공간에 위치되어 있다. 그러나 이러한 구조는 안정한 3차원 구조를 이룰 때에만 해당하며, 페로브스카이트를 구성하는 원자의 크기에 따라 다른 구조가 나타날 수도 있다. 따라서 해당 원자로 페로브스카이트가 구성되었을 때 안정한 페로브스카이트 구조를 이루는지 확인하기 위하여 2가지 파라미터를 사용하는데, 골드슈미트 공차 계수와 정팔면체 계수가 이에 해당한다. 골드슈미트 공차 계수를 구하는 방법은 다음과 같다32).
이 때 t는 골드슈미트 공차 계수를 의미하며 Ra, Rb, Rx는 각각 A, B, X의 이온 반지름을 의미한다. 일반적으로, 골드슈미트 공차 계수의 값이 0.8에서 1.0 사이일 때 정육면체의 안정적인 페로브스카이트를 이룰 수 있으며, 그 이외의 값을 가질 때는 정육면체에서 비틀어진 다른 구조를 가지게 된다24). 해당 파라미터는 이온 반지름만 가지고 구조에 대한 빠른 예측을 가능하게 하지만 모든 경우에 들어맞는 것은 아니라는 불완전한 요소를 가지고 있다. 한편, B 양이온이 정팔면체 케이지 안에 적절하게 들어갈 수 있는지 또한 고려해야 하는데 이를 고려할 수 있는 것이 정팔면체 계수이다. 정팔면체 계수를 구하는 방법은 다음과 같다33).
이 식에서, μ는 정팔면체 계수를 의미하며 Rb, Rx는 각각 B, X의 이온 반지름을 의미한다. 일반적으로 정팔면체 계수가 0.442와 0.895 사이일 경우 안정적인 페로브스카이트 구조를 이룰 수 있다고 여겨진다.
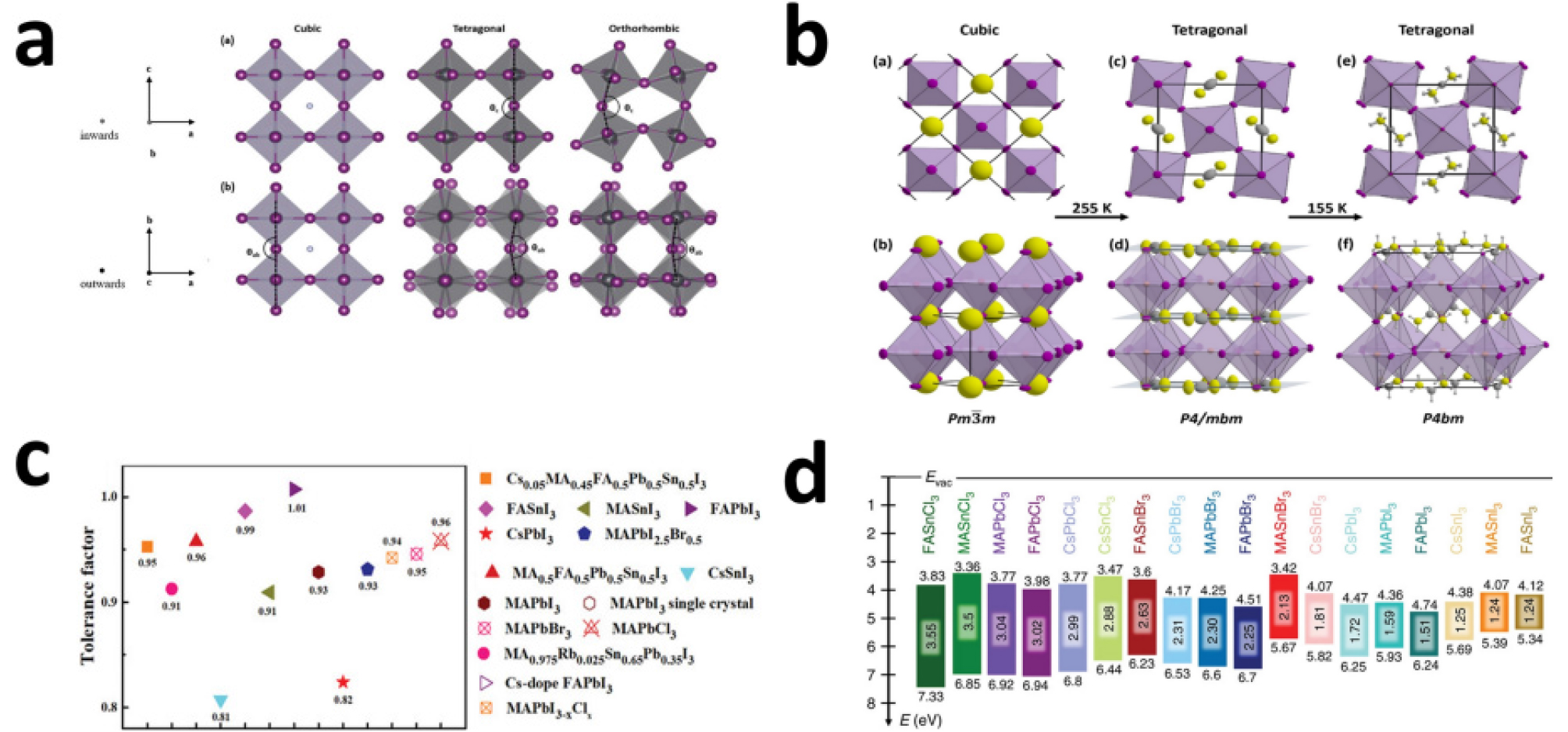
위에서 말한 이온 반지름뿐만 아니라, 온도와 [BX6]4-에서 B-X-B의 각도와 길이 또한 결정 구조에 영향을 미치는 요소이다. 예를 들어, Fig. 2a와 같이 B-X-B의 각도가 180도일 경우 페로브스카이트가 정육면체 구조를 형성하지만, 180도보다 작은 각도로 존재할 경우 직육면체 구조로 비틀릴 수 있다34).
2.2.2 주석 페로브스카이트의 상변화
A 양이온의 종류와 X 음이온의 종류에 따라 그리고 여러 종류의 이온을 혼합해 사용함에 따라 다양한 종류의 주석 페로브스카이트를 형성할 수 있다. 그러나 현재 주석 페로브스카이트 태양전지의 경향을 보면 I-만 X 음이온으로 사용하고 있기 때문에 FASnI3, MASnI3, CsSnI3 페로브스카이트에 대해서만 알아보고자 한다. Schueller와 공동 연구진들에 따르면, FASnI3 페로브스카이트는 255K 이상의 온도에서는 정육면체 구조인 Pm3m 구조로 존재하고 255K 이하의 온도에서는 정방정 구조인 P4/mbm 구조로 존재한다(Fig. 2b)35). 그리고 추가로 온도를 155K으로 낮출 경우 상변화가 한 번 더 일어나게 되며 직육면체 구조인 Pnma 구조로 존재하게 된다. 한편 MASnI3 페로브스카이트는 295K과 그 이상의 온도에서는 정육면체 구조인 Pm3m으로 존재한다. 온도를 낮춰 275K이 되면 정방정 구조인 I4/mcm으로 상변화가 일어나게 된다. 온도를 더 낮춰 온도가 110K 아래가 된다면, 직육면체 구조인 Pbn21 또는 Pbnm 구조로 상변화가 일어나게 된다36). CsSnI3 페로브스카이트는 425K 이상의 온도에서 정육면체 구조를 가지고 425K 이하 온도에서는 정방정 구조를 가지며, 350K 이하로 온도가 떨어지게 될 경우 직육면체 구조와 1차원 이중 사슬 구조가 공존하도록 상변화가 일어나게 된다37). 각각의 정육면체 구조에서 상변화 온도를 비교해보면 FASnI3, MASnI3, CsSnI3 순서로 상변화 온도가 증가하는 것을 확인할 수 있다. 이는 A 양이온의 크기 차이로 인해 나타나는 결과로, 세슘 원자의 크기가 다른 원자에 비해 비교적 작아 정육면체 페로브스카이트 구조를 형성하기에는 불안정하기 때문에 나타나는 결과이다. 이는 골드슈미트 공차 계수를 구하면 더 명확하게 알 수 있다. FASnI3, MASnI, CsSnI3 의 골드슈미트 공차 계수는 각각 0.91, 0.86, 0.82로 골드슈미트 공차 계수가 안정한 정육면체 구조임을 의미하는 1에 가까울수록 낮은 온도에서도 정육면체 구조로 안정한 것을 확인할 수 있다(Fig. 2c)38). 추가적으로 Fig. 2c에서 납 주석 페로브스카이트와 주석 페로브스카이트를 비교해 본다면, 예상과 달리 주석 페로브스카이트가 납 페로브스카이트에 비해 큰 골드슈미트 공차 계수를 가지고 더 1에 가까운 것을 확인할 수 있다. 이는 주석 페로브스카이트의 불안정성이 다른 요소에서 기인하는 것임을 의미하며, 구조적인 측면만 봤을 때는 주석 페로브스카이트가 납 페로브스카이트보다 안정한 구조를 가지고 있는 것을 의미한다. 실제로 정육면체 구조에서 정방정 구조로 상변화하는 온도를 찾아보면 MAPbI3는 330K, FAPbI3는 300K로 주석 페로브스카이트보다 높은 온도에서 상변화하는 것을 알 수 있다39).
2.2.3 주석 페로브스카이트의 전자적 특성과 광학적 특성
주석 페로브스카이트의 전자적 특성 대부분은 주석 원자의 오비탈과 아이오딘 원자 오비탈의 조합으로 인해 나타난다. 주석 페로브스카이트의 상태밀도함수 계산을 통해 주석의 5s 오비탈과 아이오딘의 5p 오비탈이 가전자대에 기여하며 주석의 5p 오비탈과 아이오딘의 5p 오비탈이 전도대에 기여하는 것을 알 수 있다40). 이러한 밴드 구조는 납의 6s 오비탈과 아이오딘의 5p 오비탈이 가전자대에 기여하며 납의 6p 오비탈과 아이오딘의 5p 오비탈이 전도대에 기여하는 것과 유사하며, 따라서 납 페로브스카이트와 마찬가지로 주석 페로브스카이트도 결함 내성을 가지고 있다. 한편, 캐리어의 유효 질량은 해당 물질의 캐리어 이동 능력에 영향을 미치는 요소로, 물질의 캐리어 유효 질량은 가전자대와 전도대의 곡률을 통해 계산할 수 있다. Table 2에서 확인할 수 있듯이, 주석 페로브스카이트의 유효 질량은 납 페로브스카이트의 유효 질량과 큰 차이가 없으며, 정공의 유효 질량이 전자의 유효 질량보다 훨씬 작기 때문에 정공의 이동이 더 빠르다는 것이 특징이다.
Table 2.
Effective masses of electrons and holes in tin and lead based perovskite, respectively
| MASnl3 | FASnl3 | MAPbl3 | FAPbl3 | |
| me* | 0.28 | 0.28 | 0.19 | 0.25 |
| mh* | 0.13 | 0.11 | 0.25 | 0.23 |
밴드 가장자리의 오비탈 조성으로 인해, 페로브스카이트의 결정 구조는 페로브스카이트의 광학적 특성에 직접적인 영향을 미친다. 모서리 공유를 하는 정팔면체 구조의 경우 정팔면체 구조가 비틀리면 더 넓은 밴드갭을 가진다는 것, 페로브스카이트의 A 양이온의 크기가 커지면 더 넓은 밴드갭을 가진다는 것, 페로브스카이트의 X 음이온의 크기가 작아지면 더 넓은 밴드갭을 가진다는 것을 그 예로 들 수 있다. Fig. 2d는 여러 주석 페로브스카이트와 납 페로브스카이트의 밴드갭과 HOMO, LUMO 에너지 준위를 나타낸 것이다34,41). Fig. 2d를 통해 주석 페로브스카이트의 차별화된 특징 2가지를 알 수 있는데, 첫 번째는 납 페로브스카이트에 비해 좁은 밴드갭을 가질 수 있다는 점이다. 아이오딘 원자만 X 음이온으로 사용한 경우 주석 페로브스카이트는 1.1-1.3eV에 해당하는 밴드갭을 가지고, 이는 단일 접합 소자에서 가장 높은 효율을 얻을 수 있는 밴드갭 영역에 해당한다. 두 번째는 납 페로브스카이트에서는 조성에 참여할 수 없는 염소 원자가 주석 페로브스카이트에선 참여 가능하다는 점이다. 이는 납 원자에 비해 주석 원자의 크기가 더 작기 때문에 나타나는 결과로, 브로민 및 아이오딘 원자보다 더 작은 염소 원자가 들어가도 비교적 안정적인 결합이 가능하기 때문이다. 높은 흡광 계수를 가지고 있다25). 그 이외에도, 납 페로브스카이트에 비해 높은 HOMO와 LUMO 에너지 준위를 가지는 것 또한 특징으로 볼 수 있으며, 이는 납 페로브스카이트 태양전지에서 사용하던 수송층보다 에너지 준위가 높은 수송층을 사용해야 할 필요성을 보여주기도 한다.
3. 주석 페로브스카이트 태양전지
앞서 언급하였듯이, 2014년 Hao와 공동 연구자들이 5.73%의 효율을 가지는 주석 페로브스카이트 태양전지를 처음 보고한 이후 다양한 엔지니어링을 통해 14.81% (인증 효율 14.03%)의 효율까지 이르렀다21-23). 지금 현재 주석 페로브스카이트는 FA 양이온이 A 위치에 존재하는 FASnI3 기반의 페로브스카이트가 주된 조성이며, 정방향 구조(n-i-p)가 아닌 역방향 구조(p-i-n)에서 더 높은 효율을 보고하고 있다. 역방향 구조의 FASnI3는 FASnI3/HTL 계면에서 전하 분리가 더 활발히 일어나 결과적으로 Sn2+/Sn4+ 산화 효과는 역방향 구조 소자보다 정방향 구조 소자에서 더 크게 나타나기 때문에 주석 기반 태양전지의 경우 역방향 구조가 정방향 구조 보다 높은 효율을 보인다42). FA+ 양이온을 주로 사용하는 이유는 다른 1가 양이온에 비해 주석의 점결함 생성에너지가 크고 외부 환경에 따른 안정성이 상대적으로 뛰어나기 때문이다23,43,44). 주석 페로브스카이트 태양전지 연구를 위해서는 주석 페로브스카이트 태양전지의 장점과 활용방안, 현재 주석 페로브스카이트 태양전지가 가지는 문제점을 아는 것이 필요하다. 따라서 이번 장에서는 위에서 말한 내용을 먼저 살펴보고 현재 존재하는 문제 해결 전략에 대해서 살펴보고자 한다.
3.1 주석 페로브스카이트 태양전지의 활용방안과 문제점
납 페로브스카이트 태양전지의 높은 효율과 다양한 안정성 및 대면적 연구에도 불구하고, 납의 독성은 상용화에 큰 걸림돌이 될 것으로 보인다 납에 대한 보다 환경 친화적인 대안으로서 주석이 주목받고 있지만, 역시 상용화가 가능한 수준의 낮은 독성을 가지는지에 대한 우려는 여전히 가지고 있다45). 한편, 1.1-1.3eV에 해당하는 밴드갭을 가진다는 것 또한 약 1.5eV의 밴드갭을 가지는 납 페로브스카이트보다 단일 접합 소자가 가장 높은 효율을 낼 수 있는 밴드갭 범위에 들어가기 때문에 장점이라고 볼 수 있다46). 또, 많은 연구가 진행 중인 다중 접합 소자를 만들 때 해당 밴드갭 영역이 하부 소자로 사용할 수 있는 영역이라는 것 또한 장점으로 생각할 수 있다.
최근 10년간 주석 페로브스카이트 태양전지가 많은 발전을 이루었으나, 산소와 물에 대한 안정성이 취약한 것은 여전히 장애물로 존재하며 상용화를 위해 필수적으로 해결해야 하는 요소이다. Fig. 3a에서 볼 수 있듯이 주석 페로브스카이트는 산소와 물에 의해 Sn2+가 Sn4+로 산화가 일어나며, Sn4+가 생성되면 자연적으로 Sn2+으로 돌아가지 않기 때문에 Sn4+가 생성되지 않는 것이 중요하다47). Sn4+로 산화되는 과정은 페로브스카이트 원료와 페로브스카이트 전구체, 페로브스카이트 필름 모든 과정에서 발생한다48). 실제로 주석 페로브스카이트 전구체를 공기 중에 노출시키면 노란색인 용액이 빨간색 용액으로 바뀌며, 주석이 산화되었음을 알 수 있다49). 주석 페로브스카이트 필름에서는 주석이 산화되는 또 다른 메커니즘이 존재하는 것을 Leijten와 공동 연구진들이 밝혔으며 그 과정을 다음과 같다.
(1) 2FASnI3 + O2 → 2FAI + SnO2 + SnI4
(2) 2FAI + SnI4 → FA2SnI6
(3) SnI4 + 2H2O → 4HI + SnO2
(4) 4HI + O2 → 2I2 + 2H2O
(5) FASnI3 + I2 → FAI + SnI4
위 과정은 Fig. 3b에 도식화하였다48). 이러한 산화는 형상구조와 광학적 및 전자적 측면에서 주석 페로브스카이트 태양전지의 성능과 안정성을 떨어뜨리는 원인이 되므로 Sn4+로의 산화를 완화시키려는 노력이 필요하다50-52).
3.2 주석 페로브스카이트 태양전지의 문제 해결 전략
3.2.1 페로브스카이트 전구체
페로브스카이트 전구체 준비 과정에서 첨가제로 인해 그리고 산소 및 물로 인해 주석의 산화가 발생할 수 있다. 이러한 산화를 막기 위해서, Fig. 3c 및 3d에서 볼 수 있듯이, 산화를 방지할 수 있는 N-Methylformanilide 및 4-acetamidophenol 와 같은 첨가제를 혼합하는 방법과 1,4-bis(trimethylsilyl)-2,3,5,6-tetramethyl-1,4 dihydropyrazine (TM-DHP) 같은 물질을 페로브스카이트 전구체에 첨가하는 방법을 이용한다49,53). 금속 주석 파우더를 사용하는 전략은 산화수가 다른 두 반응물이 중간 산화수를 갖는 화합물을 형성하는 역불균등화 반응을 이용한 것으로, Sn4+가 생성되더라도 Sn + Sn4+ → 2Sn2+ 반응을 통해 다시 Sn2+가 생성되도록 하는 전략이다. TM-DHP를 사용하는 전략은 TM-DHP가 Sn4+를 Sn0 나노입자로 변환시키는 것을 이용한 것으로, +4 산화 상태가 존재하지 않는 페로브스카이트 전구체를 얻을 수 있었고 이를 통해 0.76V의 개방전압과 11.5%의 효율을 가지는 주석 페로브스카이트 태양전지를 제작하였다.
3.2.2 주석 페로브스카이트 A 양이온 혼합
A 양이온을 혼합하여 사용하는 전략은 납 페로브스카이트 태양전지에서 높은 효율과 안정성을 위해 이미 유용하게 사용되고 있는 전략이다54). 그리고 이 방법은 주석 페로브스카이트 태양전지에도 똑같이 적용 가능하다. Liu와 공동 연구원들은 MA+와 Cs+ 양이온을 혼합해서 페로브스카이트를 제작했고 0.20V라는 낮은 개방전압으로 인해 낮은 효율을 A 양이온 혼합 초기 연구에 보고하였으나, 이후 점차 발전하여 FA+와 MA+ 양이온의 혼합을 이용해 0.61V의 개방전압과 7.14%라는 발전된 효율을 기록하였다55,56). 납 페로브스카이트 태양전지에서 잘 알려져 있듯이, A 양이온의 혼합은 A 양이온 크기가 [BX6]4- 정팔면체 사이 공간에 들어갈 수 없어 비틀린 구조를 정상적인 페로브스카이트 구조로 바꾸는 데 기여하며, 이는 소자의 효율과 안정성을 증가시킨다.
3.2.3 산화 방지제 첨가
계속 강조했듯이 주석 페로브스카이트 태양전지의 안정성의 핵심은 Sn2+의 산화 여부이다. 따라서 산화 과정을 방지하는 산화 방지제의 사용은 가장 원론적인 전략이다. Kayesh와 공동 연구진들은 클로라민(NH2Cl)을 전구체에 첨가하여 필름을 만듦으로써 FASnI3의 Sn4+의 비율을 7.3%에서 4.9%로 감소시켰으며, 동시에 페로브스카이트와 상호작용을 통해 캐리어의 재결합을 억제하였다57). 이를 통해 소자 효율은 5.4%를 달성하였고 1000시간동안 질소 상태에서 65%의 초기 효율 또한 달성하였다. Wang과 공동 연구원들은 페닐하이드라지늄 할라이드 산화 방지제를 전구체에 첨가하였고, 11.4%의 뛰어난 소자 효율과 110일의 소자 안정성을 보고하였다(Fig. 3e)58). 이러한 연구들을 보면 유기 산화 방지제가 Sn2+의 산화를 효과적으로 방지하고 있다는 것을 확인할 수 있다. 특히, 하이드라자이드 기반의 산화 방지제가 뛰어난 성능을 보이며 가장 많이 사용되고 있는 물질인 것은 주목해 볼 만한 특징이다. 최근에 하이드라자이드 기반의 산화 방지제가 환원성이 강해 전구체의 환원까지도 야기한다는 연구 결과도 있으며, 이로 인해 주석의 산화는 막으면서 전구체의 환원은 방지할 수 있는 산화 방지제에 대한 연구 또한 진행 중에 있다59).
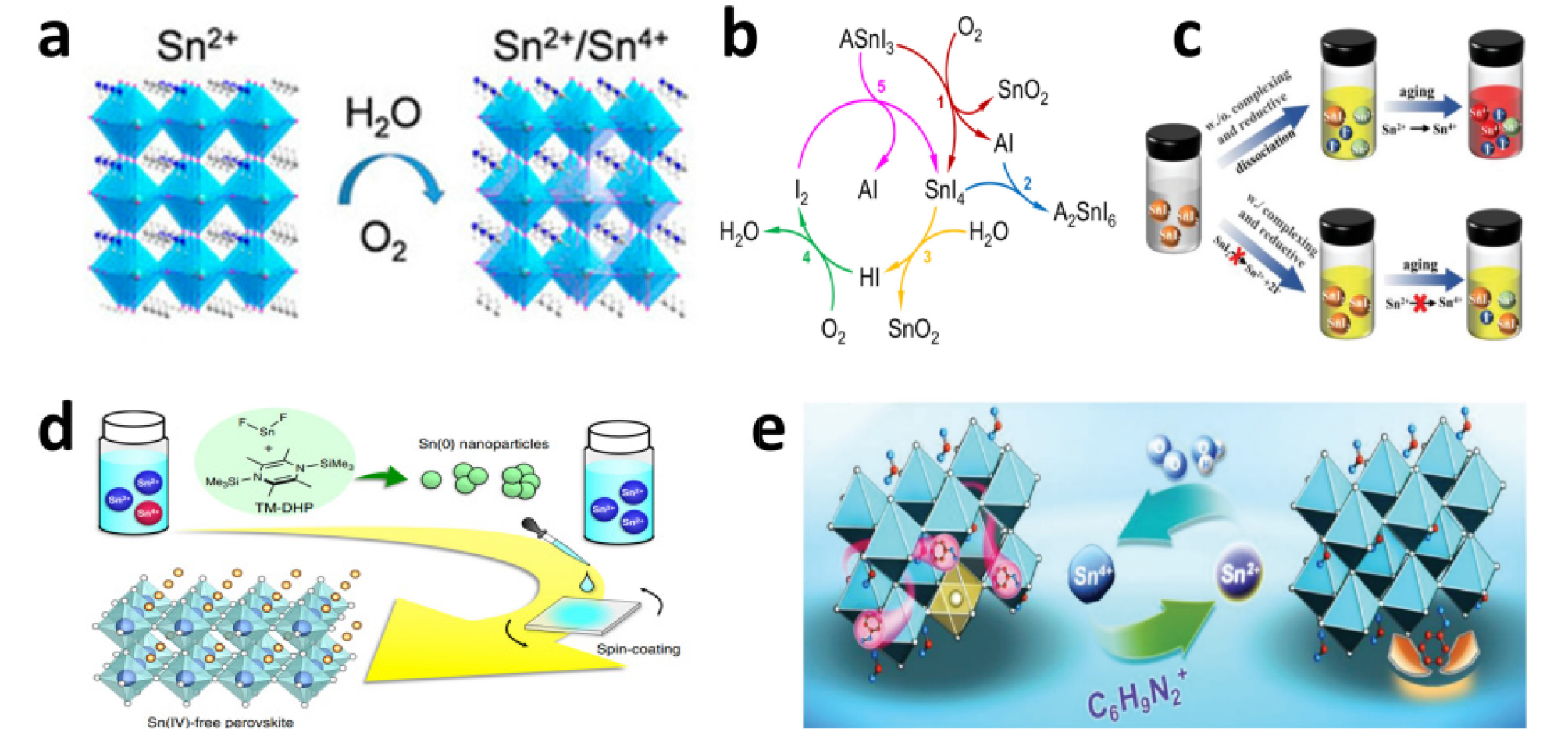
Fig. 3
(a) Oxidation of tin with oxygen and water47). (b) Oxidation process of tin perovskite48). (c) Process of adding reductive to the precursor to prevent oxidation of tin perovskite49). (d) Process of adding TM-DHP to precursor to prevent oxidation of tin perovskite53). (e) Process of suppressing oxidation of tin perovskite by adding phenylhydrazinium halide antioxidant58).
3.2.4 주석 페로브스카이트의 계면 엔지니어링
주석 페로브스카이트 태양전지는 0.4-0.9V 사이의 낮은 개방전압으로 인해 아직까지 상대적으로 낮은 효율을 보고하고 있다. 이는 주석 페로브스카이트의 주석의 산화로 인한 결과이기도 하지만 동시에 캐리어 재결합이 납 페로브스카이트 태양전지에 비해 과도하게 많기 때문에 나타나는 결과이다. 캐리어 재결합이 과도하게 많은 이유는 크게 2가지로 설명할 수 있는데, 첫 번째는 전하 및 정공수송층의 어긋난 에너지 준위이고 두 번째는 주석 페로브스카이트의 결정화이다. 주석 페로브스카이트 태양전지의 전하 및 정공수송층은 주석 페로브스카이트의 에너지 준위에 완전히 일치하는 것을 쓰는 것이 아니라, 납 페로브스카이트 태양전지에 사용했던 전하 및 정공수송층 중 괜찮은 물질을 선택해 사용하였다34,36). 따라서 납 페로브스카이트 태양전지에 비해 높은 재결합 정도를 가지게 되는 것이다. 주석 페로브스카이트의 바로 직전에 제작하는 수송층은 에너지 준위뿐만 아니라 페로브스카이트의 결정화에도 영향을 미친다. 수송층과 페로브스카이트 전구체 간 표면 에너지와 형상구조는 페로브스카이트의 결정화 속도에 영향을 줘, 주석 페로브스카이트의 형성 양상에 차이를 준다. 그 이외에도, 수송층은 페로브스카이트의 결정화를 쉽게 유도하는 불균일 결정화에도 효과가 있다.
또한, 주석 페로브스카이트의 결정화 과정은 여러 면에서 납 페로브스카이트의 결정화 과정과 다르다. 주요 차이점 중 하나는 결정화 과정에서 페로브스카이트 상의 안정성이다. 주석 페로브스카이트는 납 페로브스카이트보다 형성 에너지가 낮기 때문에 결정화 과정에서 열화 및 위상 불안정에 더 취약하다60). 결과적으로 페로브스카이트 상의 형성을 촉진하고 생성된 필름의 안정성을 향상시키기 위해 첨가제 또는 보조 용매를 사용하는 것이 필요하다. 주석 페로브스카이트의 결정화 공정은 전구체 재료의 선택과 사용된 처리 방법에 의해 영향을 받을 수 있다. 예를 들어, 전구체로 요오드화주석(IV) (SnI4) 을 사용하면 준안정 중간상이 형성될 수 있으며, 이는 페로브스카이트 상으로 전환하기 위해 추가 어닐링 단계가 필요하다. 대조적으로, 전구체로 요오드화주석(II)(SnI2)을 사용하면 결정화 동역학이 빨라지고 페로브스카이트 상의 안정성이 향상될 수 있다.
4. 결 론
이 리뷰를 통해서 먼저 주석 페로브스카이트 태양전지의 중요성과 다른 납이 없는 페로브스카이트 태양전지에 비해 뛰어난 부분, 주석 페로브스카이트 태양전지의 간략한 발전 과정에 대해서 알아보았다. 그 후 주석 원자의 기본적인 성질을 이야기하였고 특히 납 원자와의 비교를 통해 주석 페로브스카이트에 대해 더 깊게 이해할 수 있었다. 주석 페로브스카이트 부분에서는 주석 페로브스카이트의 구조와 상변화, 주석 페로브스카이트의 전자적 특성 및 광학적 특성에 대해 알아보았다. 마지막 장에서는 주석 페로브스카이트 태양전지에 대해 이야기했으며, 기대되는 활용 방안과 현재 존재하는 문제점 그리고 문제점을 해결하기 위해서 사용되고 있는/사용해야 할 전략에 대해 살펴보았다.
이 리뷰를 작성하면서 주석 페로브스카이트 태양전지가 상용화를 위해 납 페로브스카이트 태양전지만큼의 높은 효율과 안정성을 달성하기 위해 필요한 부분에 대해서 생각해 보았고, 3가지로 이를 요약해보았다. 1) FA+ 양이온이 여전히 주석 페로브스카이트의 높은 효율을 위한 주된 A자리 양이온으로 사용되고 있지만, PEA+에서 14%가 넘는 효율을 달성한 연구가 있는 것과 같이 여전히 최고 효율을 위한 적절한 조성이 밝혀지지 않았다. 이는 납과 다른 결합 세기와 다른 원자 크기를 가지고 있는 주석 원자에서 기인한 것으로, 이에 대한 더 폭넓은 연구가 필요하다. 2) 수송층은 기존의 납 페로브스카이트 태양전지에서 사용했던 수송층과 동일하기 때문에 에너지 준위가 적절하지 않다. 더 적은 재결합과 캐리어 추출을 위해서는 적절한 에너지 준위가 필요하며, 이에 대한 합성 및 엔지니어링 연구가 필요하다. 3) 현재 높은 효율을 보고하고 있는 주석 페로브스카이트 태양전지는 모두 역방향 구조이다. 이는 정방향 구조가 가장 높은 효율을 보이는 납 페로브스카이트 태양전지와는 다른 양상이다. 이에 대한 추가적인 연구가 필요하다.
높은 효율과 안정성을 달성하기 위해 언급한 필요한 3가지 부분은 쉽게 달성하기 어려운 부분이다. 그렇지만 이를 달성할 수 있을 경우 납 페로브스카이트 태양전지와 견줄 수 있는 효율과 안정성만이 아니라 페로브스카이트 태양전지의 상업화도 가능하게 될 것이다.